Pengertian Hukum Boyle, Rumus, Penerapan dan Contoh Soal – Gas adalah salah satu wujud zat yang mempunyai sifat di mana partikel-partikel penyusunnya merupakan yang paling bebas di antara zat lainnya, cair dan padat.
Kita bisa memanfaatkan kelebihan masing-masing wujud zat apabila kita memahami karakteristik masing-masing wujud zat. Kondisi sebuah gas yang berada pada sebuah ruang tertutup akan selalu mendapat pengaruh dari tiga kondisi dasar yakni suhu, volume dan tekanan.
Pengertian Hukum Boyle, Rumus, Penerapan dan Contoh Soal
Serupa dengan zat cair, zat gas akan mendapat tekanan ke semua arah dengan besar yang sama. Benda-benda seperti minyak wangi, hair spray, botol parfum dan cat pilox memanfaatkan tekanan udara yang terdapat dalam ruang tertutup. Jika ujungnya ditekan sehingga terbuka, maka zat cair di dalamnya akan keluar secara otomatis.
Pengertian Hukum Boyle
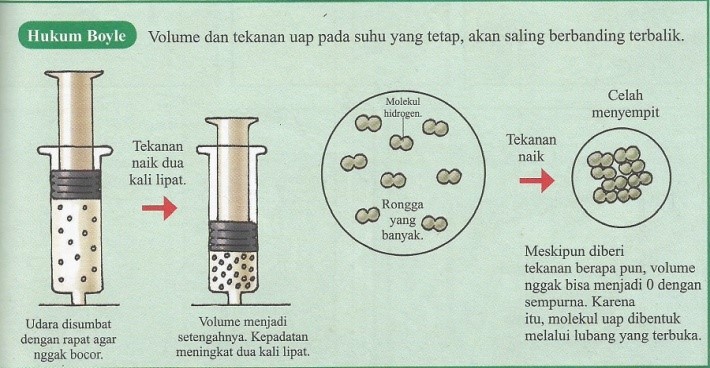
Hukum Boyle adalah sebuah teori yang dipelajari dalam ilmu fisika. Hukum Boyle menerangkan hubungan yang ada antara volume suatu gas dengan tekanan. Hukkum Boyle sendiri ditemukan oleh Robert Boyle (1627 – 1691) yang mengadakan sebuah eksperimen dengan tujuan mengetahui hubungan antara volume gas dan tekanan dalam suhu yang tetap.

Berdasarkannya eksperimennya, didapatkan hasil bahwa hasil kali volume gas dan tekanan dalam ruang tertutup ialah konstan atau tetap. Dikutip dari laman Wikipedia yaitu salah satu dari sekian banyak hukum kimia dan termasuk dalam kasus khusus dari hukum kimia ideal.
Menerangkan opisis dari hubungan proporsi antara volume gas dengan tekanan absolut jika suhu konstan dalam sistem tertutup. Merupakan hasil temua Robert Boyle meneliti adanya pengaruh tekanan pada volume gas di suhu yang konstan.
Hukum ini berbunyi “pada suhu konstan, tekanan gas dalam sebuah ruang tertutup berbanding terbalik dengan volume gas”. Salah satu alat yang menggunakan Hukum Boyle misalnya alat suntik dan pompa sepeda.
Rumus Hukum Boyle
“Pada suhu konstan, tekanan gas dalam sebuah ruang tertutup berbanding terbalik dengan volume gas” dan jika dituliskan dalam sebuah persamaan, maka akan seperti berikut.
Keterangan :
P : tekanan gas
V : volume gas
C : bilangan tetap (konstanta)
Jika tekanan diubah, maka volume gas pun mengalami perubahan dan dapat dirumuskan seperti berikut.
Hukum Boyle akan berlaku pada kondisi-kondisi tertentu. Syarat berlakunya Hukum Boyle adalah :
- Suhu yang konstan atau tetap
- Gas berada dalam ruang tertutup
- Tidak terjadi reaksi kimia
- Tidak terjadi perubahan wujud gas
Contoh Penerapan Hukum Boyle
Alat Suntik
Adalah contoh paling sederhana dalam penerapan Hukum Boyle. Pada saat batang penutup ditarik, maka volume ruang dalam tabung alat suntik akan bertambah.
Bertambahnya volume ruang membuat tekanan berkurang secara otomatis sehingga alat suntik akan menarik gas atau cairan agar kekosongan ruang bisa terisi dan tekanan dalam ruang menjadi sama.
Cat Pilox
Atau cat semprot memiliki dua jenis zat yakni cat dan gas dengan tekanan tinggi yang disebabkan tekanan oleh gaya yang amat besar di dalam kaleng. Kaleng akan dikocok terlebih dahulu agar gas dan cat menyatu. Pada saat lubang terbuka cat dan gas secara otomatis meyembur keluar sebab tekanan di dalam kaleng yang sangat besar.
Pompa
Yakni alat yang digunakan untuk memindahkan zat cair atau gas. Ada pompa hisap dan pompa tekan. Cara kerja pompa yakni pada saat penghisap ditarik, volume udara di dalam pompa naik dan udara tidak bisa masuk ke dalam ban karena harus melewati ventil (katup karet terlebih dahulu.
Penghisap yang ditekan membuat volume udara dalam pompa berkurang dan udara bisa melewati ventil sebab besarnya tekanan.
Contoh Soal
Suatu ruang tertutup diisi dengan gas bervolume 200 ml. Tekanan yang ada dalam ruang sebesar 60 cmHg, maka berapa tekanan gas dalam ruang bervolume 150 ml?
Penyelesaian :
Diketahui
Jadi, besarnya tekanan gas di ruang tertutup bervolume 150 ml adalah 80 cmHg.
Sebuah ruang tertutup bervolume 0,2 m³ memiliki tekanan gas sebesar 60.000 Pa. Carilah besarnya nilai volume gas jika tekanan gas ditambah menjadi 80.000 Pa!
Penyelesaian :
Diketahui
Jadi, besarnya volume ruang tertutup jika tekanannya 80.000 pa yaitu 0,15 m³
Suatu gas dalam ruangan tertutup mempunyai tekanan senilai P dan volumenya senilai V. Apabila gas tersebut ditekan sejumlah gaya sehingga tekanannya bertambah 5 kali lipat tekanan semula, maka berapakah nilai volume gasnya jika diketahui tidak ada perubahan suhu ?
Penyelesaian :
Diketahui
Demikianlah penjelasan materi Pengertian Hukum Boyle, Rumus, Penerapan dan Contoh Soal. semoga penjelasan tersebut mudah dipahami oleh para pembaca 🙂